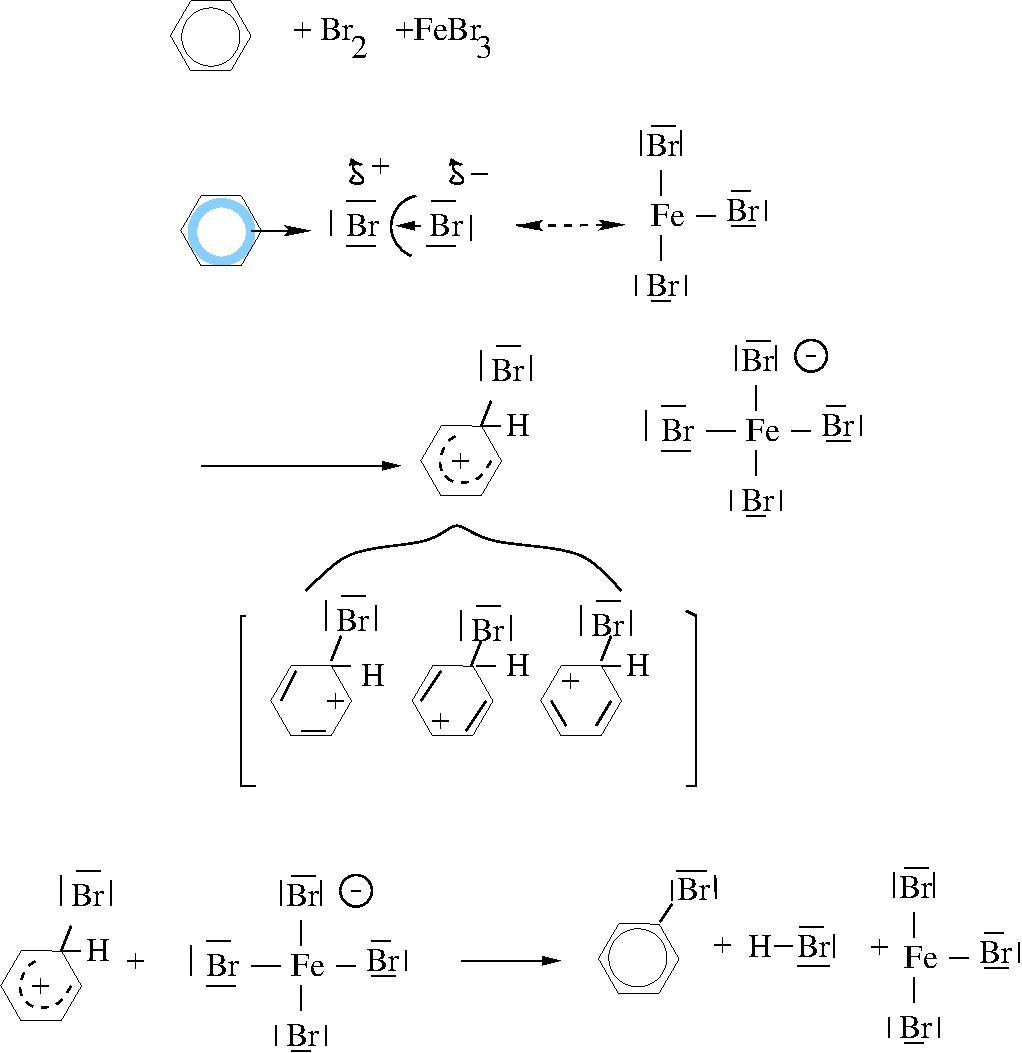
Start: Benzol und Brom
Vor dir siehst du oben ein Benzol-Molekül (C₆H₆) und ein Brom-Molekül (Br₂).
Beobachtung im Labor: Benzol reagiert nicht mit Br₂ - weder bei Raumtemperatur noch mit UV-Licht!
Zum Vergleich: Alkene (z.B. Ethen) entfärben Bromwasser sofort durch Addition. Benzol tut das nicht - warum?
Die braune Farbe des Broms bleibt erhalten. Erst mit einem speziellen Katalysator wird die Reaktion möglich!
Warum keine Reaktion?
Benzol ist außergewöhnlich stabil durch sein aromatisches System. Aber was bedeutet das genau?
Die Besonderheit: Im Benzolring gibt es 6 π-Elektronen (jeweils eines von jedem C-Atom). Diese sind nicht fest zwischen zwei C-Atomen lokalisiert, sondern über den gesamten Ring delokalisiert - sie bilden eine "Elektronenwolke" über und unter der Ringebene.
Energetischer Vorteil: Diese Delokalisierung führt zu einer Stabilisierungsenergie von ca. 150 kJ/mol (Resonanzenergie). Das macht Benzol so stabil, dass es sich völlig anders verhält als normale Alkene:
• Alkene: reagieren leicht mit Br₂ (auch ohne Katalysator)
• Benzol: reagiert NICHT einfach - es "schützt" sein aromatisches System!
ℹ️ Warum Elektronenmangelverbindung?
FeBr₃ ist normalerweise eine Ionenverbindung (Fe³⁺ und 3 Br⁻).
Im unpolaren Benzol liegt es jedoch als kovalentes Molekül vor.
Das Eisen-Atom hat dann nur 6 Valenzelektronen (3 Bindungen zu Br) statt der nach der Oktett-Regel angestrebten 8 Elektronen.
→ Dadurch kann es als Lewis-Säure ein Elektronenpaar aufnehmen!
Der Katalysator: FeBr₃
Mit Eisen(III)-bromid (FeBr₃) als Katalysator wird die Reaktion möglich!
Was ist eine Lewis-Säure? FeBr₃ ist eine Elektronenmangelverbindung - das Fe-Atom hat nur 6 Valenzelektronen (3 Bindungen zu Br) statt der angestrebten 8. Deshalb kann es ein Elektronenpaar aufnehmen.
Die Rolle des Katalysators: FeBr₃ aktiviert das Br₂, indem es die Br-Br-Bindung polarisiert. Dadurch entsteht ein elektrophiles Brom, das den stabilen Benzolring angreifen kann.
Der "Bromschleier" beginnt sich zu lichten - die nächste Reaktionsstufe wird sichtbar!
Wechselwirkung: Br₂ + FeBr₃
Der entscheidende Schritt: FeBr₃ nähert sich dem Br₂-Molekül. Eines der Brom-Atome hat freie Elektronenpaare, die das elektronenhungrige Fe-Atom anzieht.
Polarisierung: Durch diese Wechselwirkung wird die Br-Br-Bindung polarisiert. Elektronendichte verschiebt sich zum FeBr₃ hin, sodass entsteht:
• Brδ+ (partiell positiv) - wird zum Elektrophil
• Brδ-···FeBr₃ (partiell negativ, gebunden an FeBr₃)
Warum wichtig? Das Brδ+ ist jetzt positiv genug, um von der negativ geladenen π-Elektronenwolke des Benzols angezogen zu werden!
Angriff auf den Benzolring
Der elektrophile Angriff: Das polarisierte Brδ+ greift die π-Elektronenwolke des Benzols an. Die π-Elektronen sind nucleophil (elektronenreich) und werden vom positiven Brom angezogen.
Heterolytische Spaltung: Im Moment des Angriffs wird die Br-Br-Bindung heterolytisch gespalten - beide Bindungselektronen gehen zum einen Brom:
Br₂ + FeBr₃ → Br⁺ + [FeBr₄]⁻
Wichtig: Das ist KEINE radikalische Spaltung! Es entsteht ein Br⁺-Ion (Elektrophil) und ein [FeBr₄]⁻-Ion (speichert das zweite Br-Atom).
Das Br⁺ bindet sich an ein C-Atom des Rings - der σ-Komplex entsteht!
σ-Komplex (Wheland-Komplex)
Das Zwischenprodukt: Es entsteht ein positiv geladener σ-Komplex (auch Wheland-Komplex oder Arenium-Ion genannt).
Was passiert? Ein C-Atom des Rings bindet das Br-Atom kovalent (σ-Bindung). Dabei wechselt es von sp²- zu sp³-Hybridisierung - es wird tetraedrisch statt planar!
Die Ladung: Der Ring trägt jetzt eine positive Ladung (+), die über mehrere C-Atome delokalisiert ist (siehe nächster Schritt).
⚠️ Wichtig: Das aromatische System ist in diesem Zwischenprodukt zerstört! Das sp³-C unterbricht die durchgängige π-Elektronenwolke. Deshalb ist der σ-Komplex energiereich und instabil - er "will" die Aromatizität zurückgewinnen!
Mesomere Grenzstrukturen
Ladungsverteilung: Die positive Ladung im σ-Komplex ist delokalisiert - sie sitzt nicht fest an einem C-Atom, sondern ist über mehrere verteilt.
Mesomere Grenzstrukturen: Um diese Delokalisierung zu zeigen, zeichnen wir mehrere Grenzstrukturen. Im Bild siehst du drei verschiedene Darstellungen mit der positiven Ladung an unterschiedlichen Positionen.
Wichtig zu verstehen: Diese Strukturen sind KEINE verschiedenen Moleküle und existieren auch nicht nacheinander! Sie sind verschiedene "Momentaufnahmen" desselben Zustands. Die Realität ist eine Mischung (Hybrid) aller Grenzstrukturen - die Ladung ist über alle gezeigten Positionen verteilt.
Warum wichtig? Diese Delokalisierung stabilisiert den σ-Komplex. Ohne diese Stabilisierung könnte er gar nicht existieren!
Rearomatisierung
Der entscheidende Schritt: Abspaltung von H⁺ (Proton) vom selben C-Atom, das das Br gebunden hat.
Was passiert?
• Das C-Atom gibt ein H⁺ ab
• Es wechselt zurück von sp³ zu sp² (wird wieder planar)
• Die durchgängige π-Elektronenwolke wird wiederhergestellt
• Das aromatische System ist zurück!
Energetik: Die Rearomatisierung ist energetisch extrem günstig, weil ca. 150 kJ/mol Aromatizitätsenergie zurückgewonnen werden! Diese enorme Energiefreisetzung ist der Grund, warum Substitution statt Addition stattfindet.
Das H⁺ reagiert mit [FeBr₄]⁻ zu HBr + FeBr₃ (Katalysator-Regenerierung).
Endprodukt
Die Produkte: Brombenzol (C₆H₅Br) + Bromwasserstoff (HBr)
Katalysator-Regenerierung: Das [FeBr₄]⁻ reagiert mit dem abgespaltenen H⁺:
[FeBr₄]⁻ + H⁺ → FeBr₃ + HBr
Der Katalysator FeBr₃ liegt wieder unverändert vor und kann erneut wirken - das ist das Kennzeichen eines echten Katalysators!
Substitution vs. Addition: Es ist eine Substitution - ein H-Atom wurde durch ein Br-Atom ersetzt. Das aromatische System bleibt erhalten, was energetisch viel günstiger ist als eine Addition (bei der die Aromatizität verloren ginge).
Bilanz: C₆H₆ + Br₂ → C₆H₅Br + HBr (katalysiert durch FeBr₃)
Zusammenfassung: Der Mechanismus der SE
Die elektrophile Substitution (SE) am Benzol verläuft in drei Hauptschritten:
1. Aktivierung des Elektrophils:
FeBr₃ polarisiert Br₂ → Br⁺ + [FeBr₄]⁻
Das Brom wird "scharf gemacht" für den Angriff
2. Elektrophiler Angriff:
Br⁺ greift π-Elektronen an → σ-Komplex (positiv geladen)
Aromatizität ist zerstört - energiereiches Zwischenprodukt!
3. Rearomatisierung:
H⁺-Abspaltung → Brombenzol + Wiederherstellung der Aromatizität
150 kJ/mol Energie werden frei - deshalb Substitution statt Addition!
Schlüsselkonzept: Die Aromatizität ist so wertvoll, dass Benzol sie um jeden Preis zurückgewinnen will. Das macht Aromaten so besonders!
Der "Bromschleier" ist komplett verschwunden - der gesamte Mechanismus ist sichtbar!
Frage 1
Warum ist Benzol so stabil und unreaktiv?
Frage 2
Was bedeutet "Lewis-Säure"?
Frage 3
Was entsteht bei der Wechselwirkung von Br₂ mit FeBr₃?
Frage 4
Warum wird das aromatische System beim Angriff zunächst zerstört?
Frage 5
Was zeigen die mesomeren Grenzstrukturen?
Frage 6
Warum ist die Rearomatisierung energetisch so günstig?
Frage 7
Warum heißt es SUBSTITUTION und nicht ADDITION?
Frage 8
Was passiert mit dem Katalysator FeBr₃?
Frage 9
Was ist das energiereichste Zwischenprodukt?
Abschlussfrage
Welche Aussage trifft auf die Gesamtreaktion zu?
Könner-Runde: Chlorierung
Jetzt geht es um die Chlorierung von Benzol!
Der Mechanismus ist analog zur Bromierung, aber es gibt wichtige Unterschiede.
Der grünlich-gelbe "Chlorschleier" wird wieder Schritt für Schritt verschwinden.
Vergleich: Cl₂ vs. Br₂
Chlor ist elektronegativer als Brom (EN: Cl = 3,0; Br = 2,8).
Die Cl-Cl-Bindung ist stärker als die Br-Br-Bindung, aber auch polarer.
Trotzdem läuft auch diese Reaktion nur mit Katalysator ab!
Katalysator: FeCl₃ oder AlCl₃
Bei der Chlorierung werden oft FeCl₃ oder AlCl₃ als Lewis-Säuren eingesetzt.
Beide wirken nach dem gleichen Prinzip: Sie polarisieren das Cl₂-Molekül.
Polarisierung und Aktivierung
Wie bei Brom: FeCl₃ zieht Elektronendichte aus der Cl-Cl-Bindung.
Es entsteht: Clδ+-Clδ-···FeCl₃
Das Chlor-Atom mit partieller Positivladung wird zum Elektrophil.
Bildung des σ-Komplexes
Der elektrophile Angriff erfolgt analog: Cl₂ + FeCl₃ → Cl⁺ + [FeCl₄]⁻
Das Cl⁺-Ion (bzw. hochpolarisiertes Cl) greift die π-Elektronenwolke an.
Es bildet sich der kationische σ-Komplex mit gebundenem Chlor.
Stabilität des σ-Komplexes
Der σ-Komplex ist das energiereichste Intermediat der Reaktion.
Seine Stabilität wird durch Mesomerie erhöht - die positive Ladung ist delokalisiert.
Je besser diese Delokalisierung, desto stabiler der Komplex!
Mesomerie und Stabilisierung
Die drei mesomeren Grenzstrukturen zeigen die Ladungsverteilung.
In Wirklichkeit ist die Ladung über alle drei gezeigten Positionen verteilt.
Diese Delokalisierung ist der Grund, warum der σ-Komplex überhaupt existieren kann.
Rearomatisierung
Die Abspaltung von H⁺ ist der treibende Schritt.
Die Rearomatisierung gewinnt ca. 150 kJ/mol Stabilisierungsenergie zurück!
Deshalb findet Substitution statt, nicht Addition.
Produkte der Chlorierung
Chlorbenzol + HCl sind die Produkte.
Der Katalysator wird regeneriert: [FeCl₄]⁻ + H⁺ → FeCl₃ + HCl
Chlorbenzol ist ein wichtiges Zwischenprodukt in der chemischen Industrie.
Reaktivität der Halogene
Allgemeine Reaktivität bei der elektrophilen Substitution:
F₂ > Cl₂ > Br₂ > I₂
Aber: F₂ ist zu reaktiv (unkontrolliert!), I₂ zu unreaktiv.
Cl₂ und Br₂ sind in der Praxis am wichtigsten!
Könner-Frage 1
Welche Aussage über die Bindungsstärke ist korrekt?
Könner-Frage 2
Warum kann auch AlCl₃ als Katalysator verwendet werden?
Könner-Frage 3 (Vergleich)
Vergleiche: Welches Halogen bildet das stärkere Elektrophil?
Könner-Frage 4 (Transfer)
Was würde passieren, wenn man die Reaktion OHNE Katalysator durchführt?
Könner-Frage 5 (Mechanismus)
Welcher Schritt ist geschwindigkeitsbestimmend (langsamster Schritt)?
Könner-Frage 6 (Energetik)
Warum ist die Rearomatisierung energetisch so günstig?
Könner-Frage 7 (Vergleich)
Was ist der Hauptunterschied zwischen Halogenierung von Alkenen und Aromaten?
Könner-Frage 8 (Transfer)
Welche Rolle spielt [FeCl₄]⁻ im Gesamtmechanismus?
Könner-Frage 9 (Verständnis)
Warum werden in der Praxis hauptsächlich Cl₂ und Br₂ verwendet?
Könner-Frage 10 (Transfer)
Was würde passieren, wenn man versucht, das aromatische System durch Addition zu zerstören?
